GRIM-19 단백질 조절 시험
[한스경제=이소영 기자] 난치성 전신경화증을 치료할 수 있는 단백질을 규명한 국내 연구결과가 발표됐다.
조미라 가톨릭대학교 의과대학 병리학교실 교수(공동 교신저자), 박진실 가톨릭류마티스연구센터 연구교수(공동 제1저자), 정하연 의생명건강과학과 연구원(공동 제1저자) 연구팀과 박성환 가톨릭대학교 서울성모병원 류마티스내과 교수(공동 교신저자)가 전신경화증(Systemic Sclerosis)에서 미토콘드리아 이동 단백질인 ‘GRIM-19’(GRIM-19;the retinoid–IFN-induced mortality-19)가 질환 진행을 억제하는 새로운 기전임을 밝혔다.
연구팀은 "‘GRIM-19’ 단백질 조절을 통해 병인 면역세포의 억제와 섬유아세포의 미토파지 조절 매카니즘을 규명해 전신경화증의 치료 효과를 입증한 것으로, 병리 기전을 이해하고 효과적인 치료 전략을 수립하는 과학적 근거를 제공한 것"이라고 설명했다.
전신경화증은 피부뿐만 아니라 폐, 심장 등 주요 장기에 섬유화가 진행되는 난치성 자가면역질환으로 현재 근본적인 치료제가 없다. 모세혈관에도 발생해 피부가 두꺼워지고 혈액순환의 방해는 물론, 폐섬유화 발현으로 호흡에 문제를 일으켜 사망까지 이를 수 있는 질환이다.
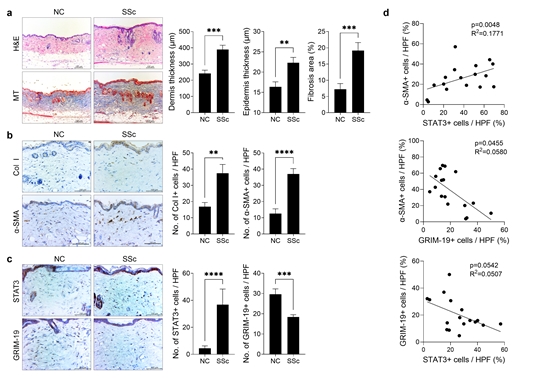
연구팀은 전신경화증에서 병증 전개 시 증가하는 전사인자 STAT3와 이의 활성을 억제하며 미토콘드리아 기능에 관여하는 GRIM-19 단백질의 상관관계를 조사했다. 전신경화증을 유도한 쥐 모델을 통해 섬유화 지표인 알파-스마(a-SMA), 콜라겐 타입1(Col I), STAT3 발현이 증가하고 GRIM-19 단백질의 수치가 감소함을 확인했다. 이는 섬유화 과정과 GRIM-19 단백질 간의 연관성을 시사하는 결과라는 설명이다.
GRIM-19 단백질의 발현을 높이는 유전자 치료를 시행해 전신경화증을 유도한 쥐에서 피부 진피의 두께가 감소하고, 염증성 사이토카인(TGF-beta, IL-6, IL-17, IL-1beta)과 섬유화 단백질(a-SMA, Col1)의 발현이 감소함을 확인했다. 또한 자가면역 병인 면역세포인 Th2, Th17 세포의 감소도 관찰됐다.
GRIM-19 단백질은 STAT3의 활성을 억제하는 것뿐만 아니라, 미토콘드리아 내로 이동해 손상된 미토콘드리아를 제거하는 ‘미토파지’ 과정을 촉진하는 역할도 하는 것으로 나타났다. 연구팀은 세포 실험을 통해 GRIM-19 단백질이 미토콘드리아 내 STAT3의 이동을 증가시키고, 이를 통해 섬유화를 억제하는 기전을 확인했다.
전신경화증 질환 모델에서 GRIM-19를 과발현시킨 결과, 손상된 미토콘드리아 제거 과정이 원활해졌으며, 섬유화 관련 단백질들의 발현이 감소하는 효과가 나타났다. 이는 GRIM-19가 미토콘드리아 기능 조절을 통해 전신경화증 치료 전략으로 활용될 수 있음을 시사한다.
박성환 교수는 “전신경화증은 약물 개발이 어려운 대표적인 난치성 질환이지만, 본 연구진이 환자 아바타 모델을 구축해 보다 정확한 타겟 치료제 개발이 가능한 상황”이라며 “미토콘드리아 이동을 유도하는 GRIM-19 유전자 치료제가 전임상 평가를 거쳐 환자에게 적용될 수 있다면 매우 유망한 치료 후보 물질이 될 것”이라고 강조했다.
조미라 교수는 “난치성 면역질환에서 면역세포와 병변 부위에서 STAT3 전사인자의 활성과 미토콘드리아 기능 이상이 관찰됐다”며 “이번 연구를 통해 규명한 GRIM-19 단백질은 이러한 문제를 동시에 조절할 수 있어, 섬유화 난치질환을 예방하거나 극복하는 데 매우 중요한 치료 타겟이 될 수 있다”고 말했다.
이소영 기자 sylee03@sporbiz.co.kr



